
Revista Científica CONAQUIC
Órgano de Investigación y Difusión de la Federación Nacional de Químicos Clínicos CONAQUIC, A.C.

Órgano de Investigación y Difusión de la Federación Nacional de Químicos Clínicos CONAQUIC, A.C.
Durante el verano del 2022 recibimos numerosos comunicados con imágenes, de colegas a lo largo de todo el país, que nos informaban de la presencia de Cyclospora cayetanensis. Situación que nos mostró que el número de pacientes se ha incrementado, también nos permitió detectar que existen dificultades para su diagnóstico y más aún que muchos nunca habían tenido la oportunidad de observarlo.
Con el propósito de contribuir a mejorar el diagnóstico de la ciclosporiosis en el laboratorio clínico, es de interés recalcar algunos detalles de la biología de Cyclospora cayetanensis y de las metodologías más frecuentemente utilizadas para su búsqueda e identificación.
Cyclospora cayetanensis es un parásito protozoario emergente, responsable de la ciclosporiosis humana, una enfermedad diarreica asociada al consumo de agua y de productos agrícolas frescos contaminados con ooquistes esporulados (Kahler et al., 2021; Sarfo et al., 2022). Los vehículos implicados en brotes de cyclosporiosis incluyen algunos alimentos que son consumidos crudos o con deficiencias en el lavado como las frambuesas, moras, fresas, arándanos, albahaca, cilantro, brotes de chícharo, germen y lechugas (Shipley et al., 2022; Mathison & Pritt, 2021). Es común observar en algunos de los supermercados leyendas en los empaques de las ensaladas para que se consuman directamente sin lavar integrando los ingredientes del contenido de la bolsa. Existen al menos 20 especies del género Cyclospora, y hasta donde sabemos sólo Cyclospora cayetanensis es la única especie que infecta a los humanos (Dubey et al., 2022).
Cyclospora cayetanensis se encuentra en todo el mundo, con una prevalencia general del 3,6% (Li et al., 2020). Es altamente endémica en regiones tropicales y subtropicales con saneamiento deficiente (Mathison & Pritt, 2021), presenta una estacionalidad variada que puede verse afectada por la precipitación, la temperatura, la humedad (Mathison & Pritt, 2021; De La Luz Galván-Ramírez et al., 2019; Frickmann et al., 2021; Sarfo et al., 2022) y quizás el fotoperiodo (Almeria et al., 2019). En México se han informado prevalencias de 2,9% en población general (De La Luz Galván-Ramírez et al., 2019) y 0.67% en niños escolares (Orozco-Mosqueda et al., 2014).
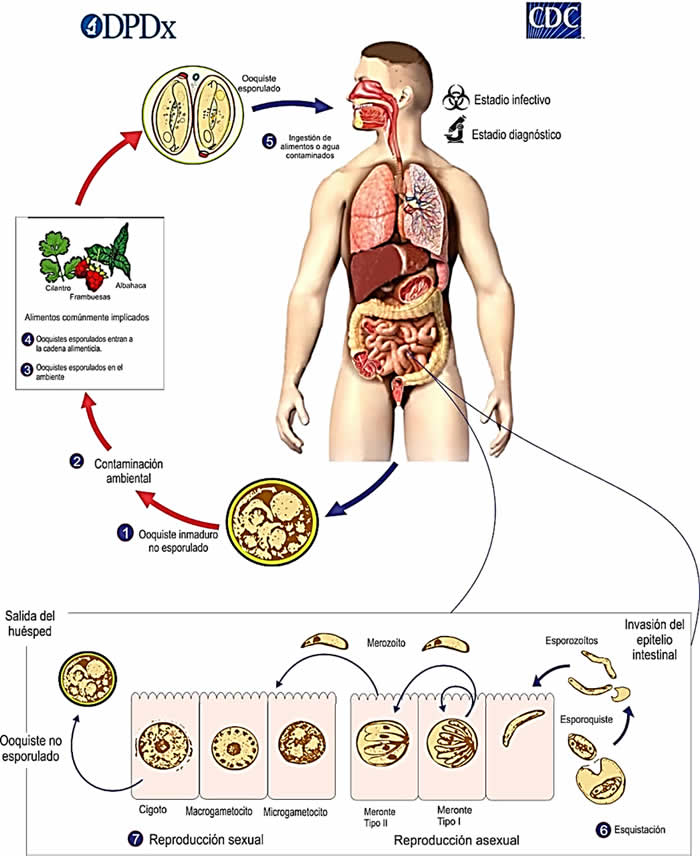
Ciclo de vida (Figura 1)
Cuando es expulsado el ooquiste en las heces no es infeccioso (1). En el medio ambiente (2) cuando tiene disponibilidad de oxígeno, la esporulación ocurre de una a dos semanas con temperatura entre 22°C y 32°C, lo que da como resultado la división del esporonte en dos esporoquistes, cada uno con dos esporozoítos alargados (3), es un proceso aeróbico. Los ooquistes esporulados pueden contaminar los alimentos frescos y el agua (4) que se ingieren (5). Los ooquistes al ser ingeridos por el humano se desenquistan en el tracto gastrointestinal, liberando los esporozoítos, que invaden las células epiteliales del intestino delgado (6). Dentro de las células se multiplican asexualmente en merontes tipo I que contienen de 8 a 12 merozoítos y merontes tipo II que contienen cuatro merozoítos. Los merozoítos de merontes de tipo I probablemente permanecen en el ciclo asexual, perpetuando la infección, mientras que los merozoítos de merontes de tipo II se desarrollan sexualmente en macrogametocitos y microgametocitos tras la invasión de otra célula huésped. Un microgametocito fertiliza a un macrogametocito, dando como resultado la formación de un cigoto que se convierte en un ooquiste, que se elimina en las heces (7) (CDC, 2019; Mathison & Pritt, 2021; Sarfo et al., 2022).
Cyclospora cayetanensis se establece como una infección en el tracto intestinal superior, que es de curso limitado en huéspedes inmunocompetentes (Sarfo et al., 2022) o causar enfermedad diarreica de tiempo más prolongado y grave en lactantes, ancianos e individuos inmunocomprometidos (Mathison & Pritt, 2021). El período de incubación promedio es de cinco a siete días (con un rango de 2 a ≥2 semanas) y puede prolongarse durante semanas a meses sin tratamiento. Los principales síntomas de la cyclosporiosis son: diarrea acuosa voluminosa, calambres abdominales, náuseas, febrícula, fatiga y pérdida de peso (Almeria et al., 2019).
La invasión y replicación del parásito dentro de los enterocitos daña el epitelio del intestino delgado, lo que lleva a la destrucción del borde en cepillo, la pérdida de las enzimas digestivas unidas a la membrana, adelgazamiento y atrofia de las vellosidades intestinales. En la lámina propia se produce una afluencia de linfocitos, células plasmáticas y en ocasiones, eosinófilos. Estos cambios tienen el efecto general de disminuir la capacidad de absorción del intestino delgado, lo que conduce a una menor absorción de agua, nutrientes y electrolitos (Mathison & Pritt, 2021).
Entre individuos inmunocomprometidos, las complicaciones que pueden surgir incluyen diarrea crónica, síndromes de malabsorción y la hiperplasia de las criptas (Sarfo et al., 2022). En pacientes con infección por VIH puede causar una infección ectópica del árbol biliar y colecistitis aguda acalculosa (Ynés R. Ortega & Sánchez, 2010; Mathison & Pritt, 2021).
Además, se encontró que las infecciones por Cyclospora cayetanensis están relacionadas con algunas otras enfermedades, incluido el síndrome de Reiter (síndrome de artritis reactiva), síndrome de Guillain-Barre (Li et al., 2020) y cáncer colorrectal en asociación con Cystoisospora belli (Mahmoudvand et al., 2019).
Se clasifica como coccidio, dentro del phylum Apicomplexa, familia Eimeriidae (Dubey et al., 2022). Los ooquistes no esporulados en frotis de heces frescas son esféricos, refráctiles y miden de 8 a 10 µm de diámetro (García et al., 2018). La doble pared del ooquiste es delgada (<1 µm) e incolora. La pared interna encierra una masa central indivisa llamada esporonte, el cual casi llena el ooquiste y tiene muchos glóbulos de diferentes tamaños (Figura 2 A).
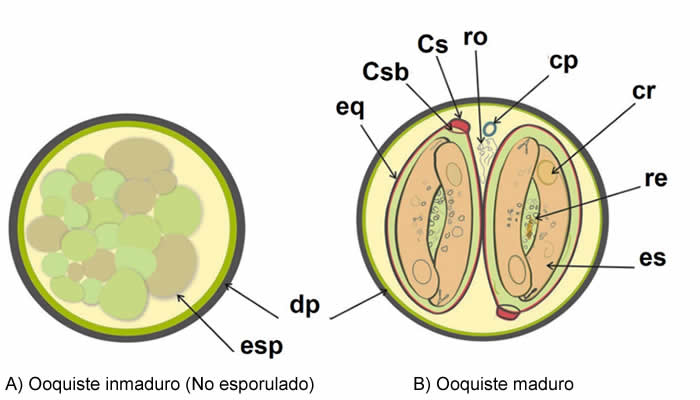
Los ooquistes completamente esporulados, contienen dos esporoquistes, cada uno con dos esporozoítos. Los esporoquistes son ovoides, ~4 × 6 µm, y contienen cuerpos de Stieda y substieda, y un gran residuo. Los cuerpos de Stieda son estructuras en forma de tapón involucradas en la exquistación de esporozoítos. Los esporozoitos son alargados, ~1 × 9 µm (Dubey et al., 2022), (Almeria et al., 2019), (Ynés R. Ortega & Sánchez, 2010), (Y. R. Ortega et al., 1994) (Figura 2 B).
La fuerte autofluorescencia azul pálido de los ooquistes de Cyclospora cayetanensis cuando se observan por microscopía ultravioleta a 365 nm (Figura 3 B), o color verde (Figura 3 C) bajo excitación de 450–490 nm (García, Lynne Shore 2021), es una condición útil para su identificación, sobre todo cuando se analizan muestras como vegetales, frutas o agua, en donde pueden estar presentes otros coccidios.
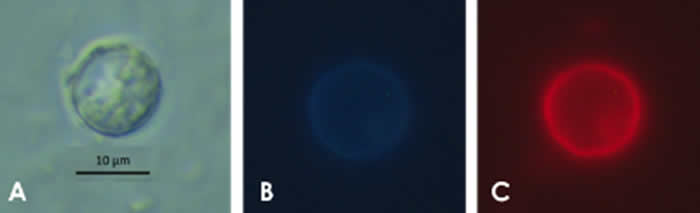
Se puede realizar en el laboratorio el proceso de esporulación de los ooquistes, agregando en partes iguales una solución de dicromato de potasio al 2,5 % (el cual disminuye el crecimiento microbiano que compite por el oxígeno), mantener a temperatura de 23 a 30°C y agitar ocasionalmente durante dos días. Esto ayuda notablemente en la identificación.
El diagnóstico presuntivo se basa en los síntomas clínicos (Li et al., 2020) y el diagnóstico confirmativo por el laboratorio, depende en gran medida del examen coproparasitoscópico, que aporta evidencias que pueden confirmar, reorientar y hacer el seguimiento de la infección (Mathison & Pritt, 2021).
El diagnóstico en el laboratorio se basa en la observación de ooquistes no esporulados en observación en fresco con solución salina y directo con yodo Lugol, tinciones diferenciales o microscopía de fluorescencia (Li et al., 2020; Frickmann et al., 2021). Las observaciones se pueden realizar directamente a partir de heces frescas o muestras concentradas mediante técnicas de sedimentación con formalina-éter o de flotación con sacarosa que aumenta la eficiencia de detección en muestras de heces con pequeñas cantidades de ooquistes (Li et al., 2020). Dado que los ooquistes se eliminan de forma discontinua, se deben recolectar al menos tres muestras de heces en días alternos (Li et al., 2020; Almeria et al., 2019).
Actualmente, no existen ensayos de detección de anticuerpos o antígenos para el diagnóstico clínico de rutina de la cyclosporiosis (Mathison & Pritt, 2021; Li et al., 2020) y las técnicas moleculares existentes son pruebas de laboratorio para la verificación de muestras clínicas sospechosas, pero representan costos elevado (Li et al., 2020) ya que deben utilizar más de una muestra.
Las técnicas de examen en fresco y teñida con yodo Lugol son más rápidas de realizar y han demostrado que pueden ser de utilidad para una evaluación inicial de rutina (Kimura et al., 2004) seguida de una técnica de concentración y, en caso de no tener aún la certeza de si identificación, utilizar técnicas de tinción permanentes.
Examen directo en fresco
Los ooquistes no esporulados de Cyclospora en heces frescas se identifican fácilmente como entidades esféricas, refringentes y que tienen un tamaño de 8 a 10 μm (Ynés R. Ortega & Sánchez, 2010; Y. R. Ortega et al., 1994; Li et al., 2020) (Figura 4).
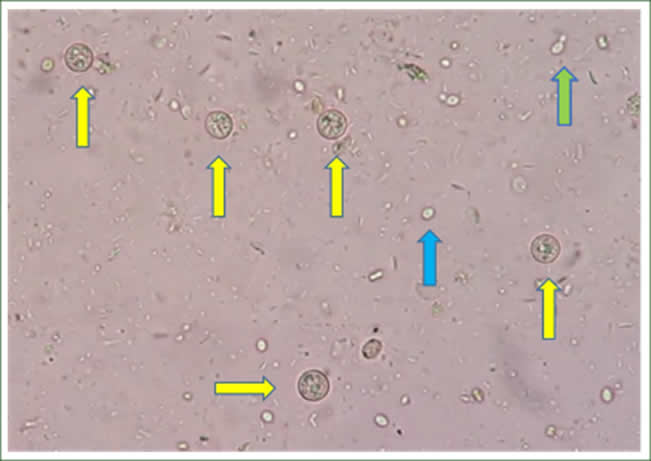
Examen directo teñido con yodo Lugol
La tinción con soluciones de yodo Lugol al 1% con no más de dos semanas de preparación y que se ha mantenido a la oscuridad en frasco ámbar permite observar con más detalle la doble pared y los glóbulos de diferentes tamaños (Figuras 5 A, B y C). Cuando se usa yodo Lugol más concentrado puede dificultar la identificación (Figura 5 D). En muestras con biliverdina, los ooquistes se observan con detalle (Figura 5 E) sin necesidad de USAR algún colorante.
Las muestras fijadas con formol (10%) al menos por 30 minutos, ayuda a transparentar el ooquiste, observándose perfectamente la doble pared. (Figura 5 E).
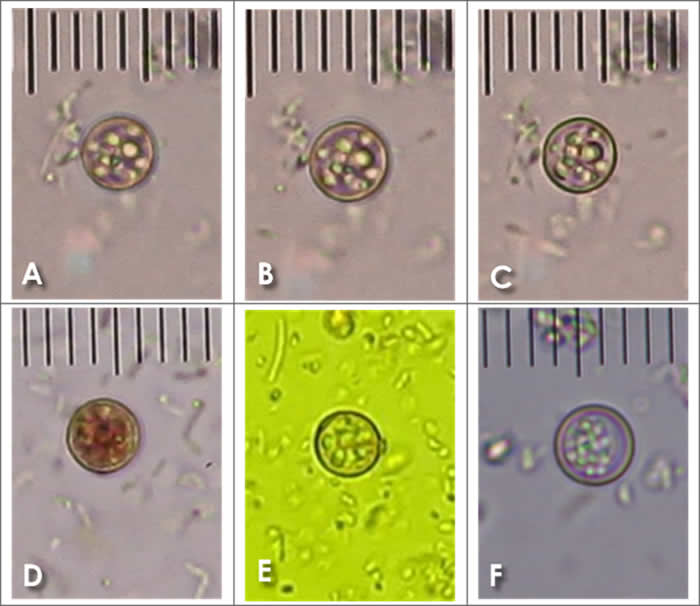
En general, las características identificadas con la tinción con yodo Lugol y la micrometría permiten identificar a Cyclospora cayetanensis, pero en casos de aún tener dudas se deben realizar tinciones permanentes, en donde la más utilizadas son la técnica de Ziehl Neelsen modificada, comúnmente denominada Kinyoun.
Tinción permanente
La detección de Cyclospora cayetanensis puede mejorarse mediante el uso tinciones permanentes como las ácido resistente de Ziehl-Neelsen modificado (OPS, 2019), también llamada técnica de Kinyoun (Shore Garcia, 2021). Los ooquistes se tiñen de forma variable con apariencia arrugada, algunos ooquistes se tiñen de rojo oscuro, mientras que otros se tiñen de rosa pálido o no se tiñen (Ynés R. Ortega & Sánchez, 2010; Mathison & Pritt, 2021). En particular con Cyclospora es posible que un gran porcentaje de ooquistes no absorban el colorante uniformemente; por lo general, hay muchas células fantasma que parecen similares a las teñidas con tricrómico (Mathison & Pritt, 2021; García et al., 2018) Figura 6.
En la tinción de Ziehl-Neelsen utilizada en el diagnóstico de la tuberculosis (OPS, 2018) se utiliza carbol fucsina a menor concentración (0.3%), fenol (5%), es necesario calentar durante la tinción el carbol fucsina y la decoloración se realiza con alcohol ácido (ácido clorhídrico al 3% en alcohol etílico o con ácido sulfúrico al 25% durante tres minutos. Mientras que la técnica de Ziehl Neelsen modificada (OPS, 2019) o Kinyoun (Shore Garcia, 2021), para la tinción de ooquistes, utiliza carbol fucsina más concentrada (3.3%) y fenol (6.6%), no es necesario calentar y la decoloración se realiza con ácido sulfúrico al 1% y el tiempo de diferenciación es reducido (sólo se decolora hasta que el flujo pierda el color rosado).
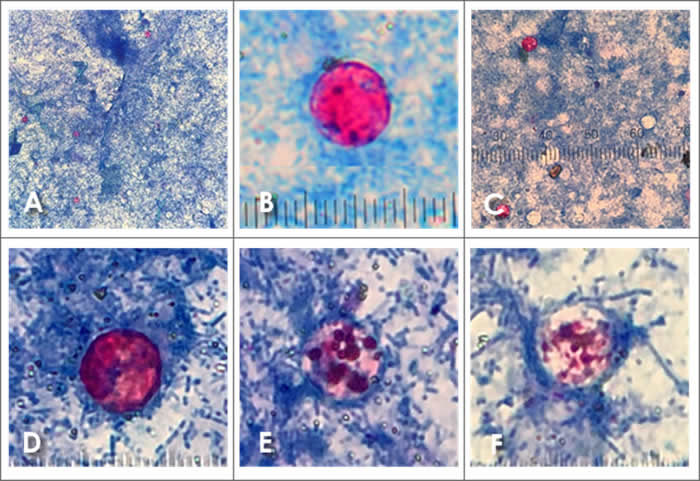
Existen otras técnicas de tinción disponibles para observar la presencia de los ooquistes de Cyclospora cayetanensis (OPS, 2021; Shore Garcia, 2020), como es la tinción con Giemsa, Safranina caliente, sin embargo nuestro grupo no ha podido reconocer alguna ventaja de estas tinciones sobre el empleo de la técnica de Ziehl Neelsen modificada.
Cuando el frotis fecal y la tinción se calientan mediante tratamiento con microondas o cuando los portaobjetos se calientan a 85 °C durante 5 min usando un baño de agua (Ynés R. Ortega & Sánchez, 2010), la tinción de safranina caliente da como resultado una tinción más uniforme (98%), ya que no se observan las estructuras esféricas sin teñir que son comunes en la tinción de Kinyoun. Los ooquistes que aparecen de color rosa a rojo o naranja y tienen un aspecto arrugado, similar a lo que se observa con los métodos Zieh-Neelsen modificado (Mathison & Pritt, 2021; Ynés R. Ortega & Sánchez, 2010), Figura 7 (A–D).
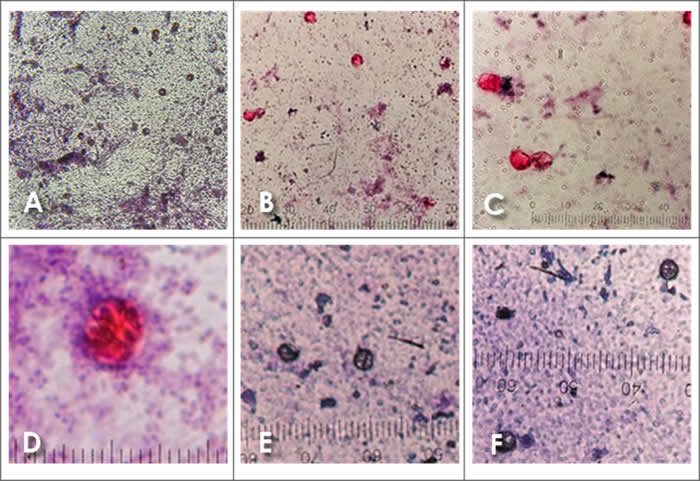
La tinción con Giemsa también revela la presencia de estructuras de los ooquistes de Cyclospora cayetanensis, los cuales se observan un poco más teñidos que el campo que lo rodea, por lo que resaltan poco, por lo que no recomendamos su empleo, Figura 7 (E –F).
Examen de concentración por centrifugación
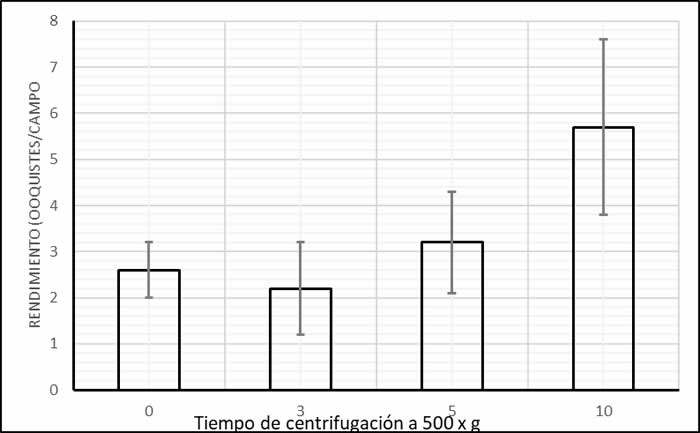
El empleo de la centrifugación por 10 minutos a 500 x g aumenta la probabilidad del hallazgo de los ooquistes (Figura 8), además a partir del sedimento se pueden realizar tinciones permanentes, por lo que es ampliamente necesario utilizar los métodos de concentración por flotación o por sedimentación, en especial en muestras de consistencia líquida y moco abundante.
Trimetoprim/sulfametoxazol (TMP/SMX) es el tratamiento de primera opción para la ciclos-poriasis (CDC, 2019; Li et al., 2020). En niños, la dosis administrada es de 5/25 mg/kg/vía oral 2 veces al día/7 días (OPS, 2019); adultos, 160/800 mg vía oral 2 veces por día por 7 a 10 días (OPS, 2019). El tratamiento administrado de esta manera, ha demostrado que proporciona tasas de curación >90% en pacientes inmunocompetentes (Mathison & Pritt, 2021). Otras opciones son la ciprofloxacina en dosis de 500 mg vía oral 2 veces al día por 7 días o nitazoxanida, 500 mg vía oral cada 12 h por 7 días (OPS, 2019). La nitazoxanida o la ciprofloxacina se recomiendan para los pacientes que no pueden tomar TMP/SMX debido a la alergia a las sulfas, aunque el tratamiento es menos eficaz (Mathison & Pritt, 2021; Li et al., 2020).
El cotrimoxazol se usa de manera profiláctica y terapéutica entre las personas que viven con SIDA en entornos de recursos limitados (Sarfo et al., 2022). En pacientes con enfermedades gastrointestinales las pruebas para Cyclospora cayetanensis no se realizan de manera rutinaria. Por lo tanto, el diagnóstico y el tratamiento adecuados no siempre se llevan a cabo con prontitud (Orozco-Mosqueda et al., 2014).
Las medidas preventivas se centran en mejorar el saneamiento para evitar que las heces humanas entren en el medio ambiente y contaminen los alimentos y el agua, así como el tratamiento de los alimentos para inactivar los ooquistes contaminantes. Los ooquistes son altamente resistentes a los desinfectantes de uso común, pero se inactivan al cocinarlos (Mathison & Pritt, 2021).
Rodríguez-Parra Kathia L
Álvarez-Fernández Blanca E
Facultad de Ciencias Químico Biológicas de la Universidad Autónoma de Guerrero, Av. Lázaro Cárdenas, S/N. Ciudad Universitaria, 39090, Chilpancingo, Guerrero, México.
Baltasar–González Miguel Ángel
Zamora–Domínguez Jorge Antonio
Laboratorio Central, Hospital General de México, “Eduardo Liceaga”. CDMX.
Álvarez–Lara Beatriz
Sánchez-Manzano, Rosa María
Miranda-Ruelas Diego Ángel
Nogueda-Torres Benjamín*
Departamento de Parasitología, Escuela Nacional de Ciencias Biológicas-IPN, CDMX.
Correspondencia:
Nogueda-Torres Benjamín*
E-mail: bnogueda@ipn.mx
Introducción del autor
